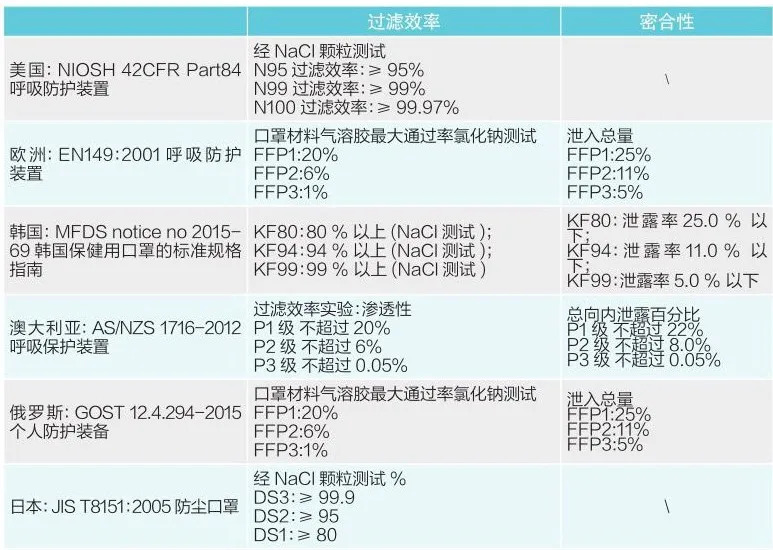
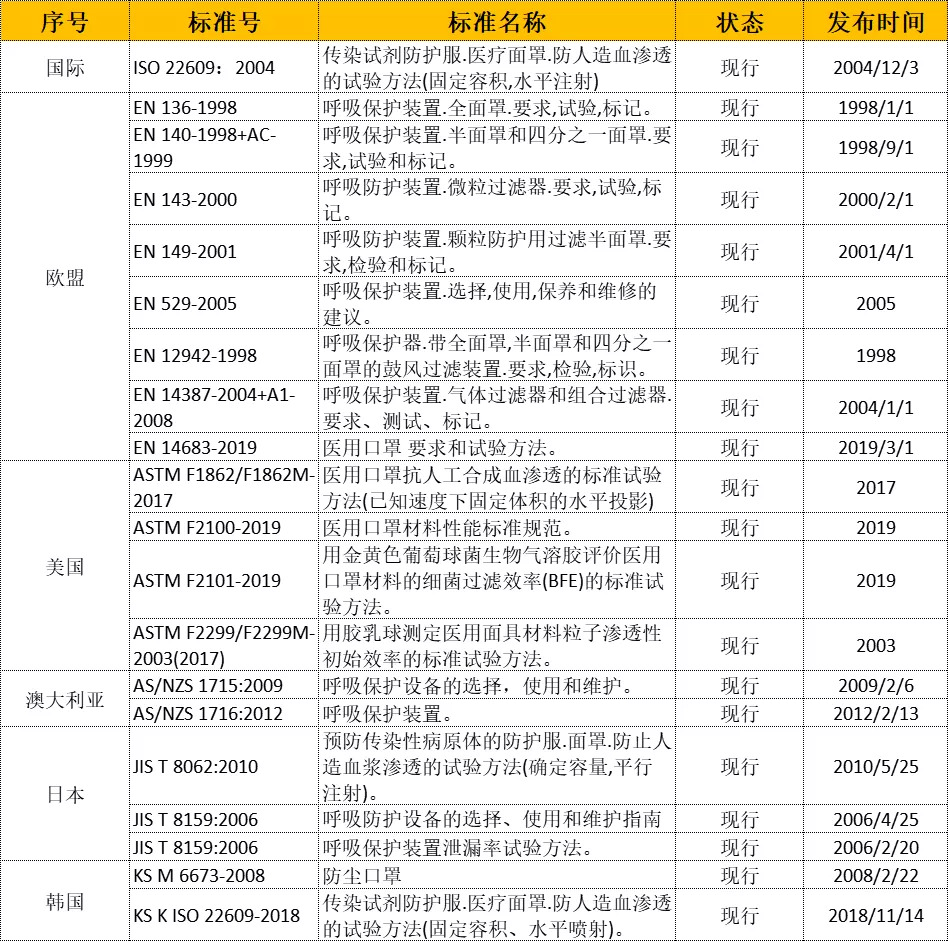
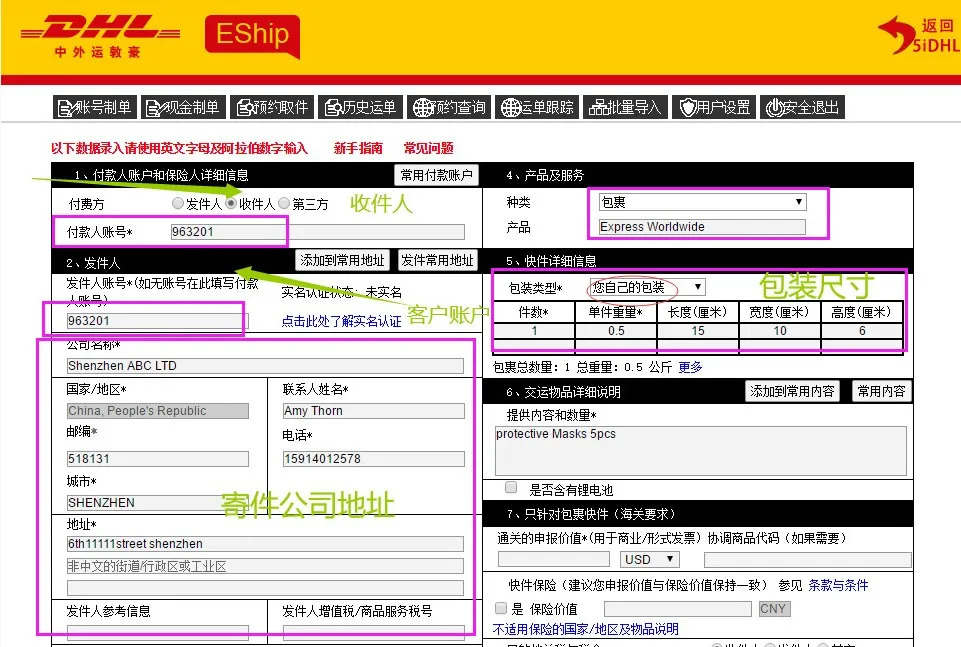
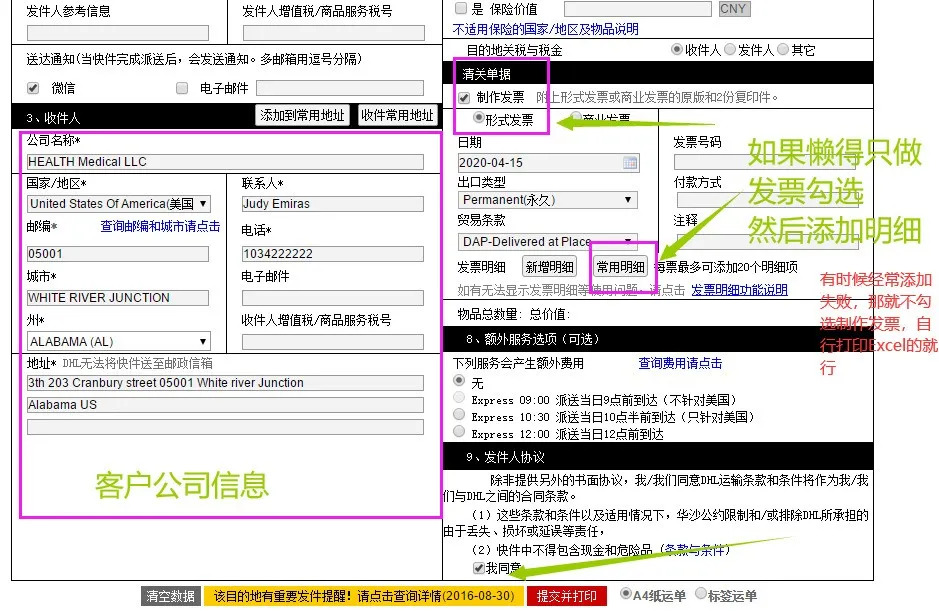
进口化妆品许可申请分为两类:普通类化妆品和特殊类化妆品,所以在我们操作进口备案的时候首先要区分我们是普通的还是特殊类的,以下是我司操作化妆品进口清关常见的一些化妆品分类
普通类:发用产品、一般护肤用品、易触及眼睛护肤用品、一般彩妆品、护唇及唇部彩妆品、指(趾)甲用品、芳香品
特殊类:育发类、健美类、美乳类、染发类、烫发类、防晒类、除臭类、祛斑类、脱毛类
进口特殊化妆品注册
一、申报流程
(一)在华申报责任备案

(二)产品检测

(三)报批过程

二、主要检测项目及第三方收费参考
表1-1 特殊用途化妆品检测项目和第三方收费标准


表1-2 特殊用途化妆品检测项目和第三方收费标准(续)


注:“O”表示需要进行检测的项目;“*”涂染暂时性染发剂不进行该两项试验。
1.产品配方中没有微生物抑制作用成分者(如物理脱毛类产品、纯植物染发类产品等)需测微生物指标。
2.乙醇、异丙醇含量之和≥10%的产品需测甲醇,费用1000元。
3.凡紫外线吸收剂(二氧化钛和氧化锌除外)含量≥0.5%的产品,需加测紫外线吸收剂、皮肤变态反应试验和皮肤光毒性试验。
4.凡宣称含有α-羟基酸或不宣称含有α-羟基酸,但其总量≥3%的产品需测定α-羟基酸,同时测定pH值,测α-羟基酸1000元,测pH值100元。
5.称祛痘、除螨、抗粉刺等功能的产品需要测抗生素和甲硝唑指标,费用1000元。
6.宣称去屑功能的产品需要测去屑剂指标,费用1000元。
7.即洗类产品不需要进行多次皮肤刺激性试验,只进行急性皮肤刺激性试验。
8.染发类或可选用体外哺乳动物细胞基因突变试验。
9.防晒类化妆品的检测时限不包括防水性能人体试验和长波紫外线防护指数(PFA值)人体试验测定时间。
10.检验数量是针对每包装净重大于25克的产品而言,不满25克者,需增加样品数量。
表2-1 防晒效果试验检测项目和第三方收费标准

表2-2防晒效果试验检测项目和第三方收费标准(续)

注:防晒类化妆品必须测定防晒指数(SPF值),并在产品上标注SPF值。
1.防晒化妆品若宣传防水效果,只可标识经防水性能测试后的SPF值;防水性能测试前后的SPF值相差若大于50%,则该产品不得标识具有防水功能。
2.根据产品宣称的抗水程度或时间选择不同测定方法。
3.可以根据所测PFA值在产品上标识PA等级:PFA值小于2,无UVA防护效果;PFA值2-3,PA+;PFA值4-7,PA++;PFA值8或8以上,PA+++。
4.PA等级或PFA值必须与SPF值同时标识。
5.若标识广谱防晒或UVA防护效果,也必须与SPF值同时标识。
三、申报资料清单
(一)进口特殊用途化妆品行政许可申请表;
(二)产品中文名称命名依据;
(三)产品配方;
(四)生产工艺简述和简图;
(五)产品质量安全控制要求;
(六)产品原包装(含产品标签、产品说明书);拟专为中国市场设计包装的,需同时提交产品设计包装(含产品标签、产品说明书);
(七)经国家食品药品监督管理总局认定的许可检验机构出具的检验报告及相关资料;
(八)产品中可能存在安全性风险物质的有关安全性评估资料;
(九)申请育发、健美、美乳类产品的,应提交功效成份及其使用依据的科学文献资料;
(十)已经备案的行政许可在华申报责任单位授权书复印件及行政许可在华申报责任单位营业执照复印件并加盖公章;
(十一)化妆品使用原料及原料来源符合疯牛病疫区高风险物质禁限用要求的承诺书;
(十二)产品在生产国(地区)或原产国(地区)生产和销售的证明文件;
(十三)可能有助于行政许可的其他资料;
(十四)产品技术要求的文字版和电子版。
*另附许可检验机构封样并未启封的市售样品1件。
四、申报资料主要要求
(一)申报资料的一般要求
1、首次申请特殊用途化妆品行政许可提交申报资料原件1份、复印件4份,复印件应清晰并与原件一致。
2、除检验报告、公证文书、官方证明文件及第三方证明文件外,申报资料原件应由申请人逐页加盖公章或骑缝章;进口化妆品(新原料)申报资料原件还应由行政许可在华申报责任单位逐页加盖行政许可在华申报责任单位公章或骑缝章。
3、使用A4规格纸张打印,使用明显区分标志,按规定顺序排列,并装订成册。
4、使用中国法定计量单位。
5、申报内容应完整、清楚,同一项目的填写应当一致。
6、所有外文(境外地址、网址、注册商标、专利名称、SPF、PFA或PA、UVA、UVB等必须使用外文的除外)均应译为规范的中文,并将译文附在相应的外文资料前。
7、终止申报后再次申报的,还应说明终止申报及再次申报的理由;不予行政许可后再次申报的,应提交不予行政许可(变更/延续)决定书复印件,并说明再次申报的理由,同时还应提交不予行政许可原因是否涉及产品安全性的书面说明。
8、产品配方应提交文字版和电子版。
9、文字版和电子版的填写内容应当一致。
10、生产和销售证明文件、质量管理体系或良好生产规范的证明文件、不同国家的生产企业同属一个集团公司的证明、委托加工协议等证明文件可同时列明多个产品。这些产品如同时申报,一个产品使用原件,其他产品可使用复印件,并书面说明原件所在的申报产品名称;这些产品如不同时申报,一个产品使用原件,其他产品需使用经公证后的复印件,并书面说明原件所在的申报产品名称。
11、产品技术要求电子版应登录国家食品药品监督管理总局化妆品行政许可网上申报系统填写。
(二)申报资料的具体要求
1、逐项提交各项资料。
2、应按照申请表填表说明的要求填写申请表各项。
行政许可申请表保证书应由进口化妆品生产企业或进口化妆品新原料生产企业法定代表人或其授权的该生产企业的签字人或其授权的行政许可在华申报责任单位的签字人签字;无公章的,应在保证书生产企业签章处予以注明。
行政许可申请表承诺书应由行政许可在华申报责任单位法定代表人或法定代表人授权该单位的签字人签字并加盖行政许可在华申报责任单位公章。
授权委托签字时,应提供授权委托书公证件及其中文译文,并做中文译文与原文内容一致的公证。根据《化妆品行政许可申报资料要求》(以下称《资料要求》)第二十四条的要求,在每次提交行政许可申请时应同时提交授权委托书原件或经公证后的复印件,并书面说明委托签字授权书原件所在的申报产品名称。授权委托签字的内容不应包含于行政许可在华申报责任单位授权书中。
3、产品配方应包括许可检验机构对进口产品配方的确认证明,其确认日期应与检验样品的受理日期一致。
4、产品质量安全控制要求应包括在原产国执行的产品质量安全控制要求(外文版及中文译文)及产品符合《化妆品卫生规范》要求的承诺。
5、因体积过小(如口红、唇膏等)而无产品说明书或将说明内容印制在产品容器上的,应在申报资料中产品包装部分提交相关说明。
6、经国家食品药品监督管理总局认定的许可检验机构出具的检验报告及相关资料或境外实验室出具的防晒指数(SPF、PFA或PA值)检验报告应符合以下要求:
(1)许可检验机构出具的检验报告,应当包括以下资料:
1) 检验申请表。
2) 检验受理通知书。
3) 产品使用说明。
4) 卫生安全性检验报告(微生物、卫生化学、毒理学)。
5) 如有以下资料应当提交:
① 人体安全性检验报告(皮肤斑贴、人体试用试验);
② 防晒指数SPF、PFA或PA值检验报告;
③ 其他新增项目检测报告(如化妆品中石棉检测报告等)。
(2)使用境外实验室出具的防晒指数(SPF、PFA或PA值)检验报告的,应当提交如下资料:
1) 出具报告的实验室已经过实验室资格认证的,应提交资格认证证书;
2) 出具报告的实验室未经过实验室资格认证的,应提交实验室严格遵循《良好临床操作规范》(Good Clinical Practice, GCP)或《良好实验室操作规范》(Good Laboratory Practice, GLP)的证明;
3) 其他有助于说明实验室资质的资料。
凡首次提交境外检验报告的,应提交上述资料的原件或经出具报告的实验室所在国(地区)行业协会、中国使(领)馆、公证处认可的复印件的确认件(含翻译件),国家食品药品监督管理总局认可后,再次申报时只需提交复印件。
境外实验室检验报告应当提交原件,系列产品符合抽检要求的,至少一个产品提交原件,其他产品可提交复印件,并说明原件所在的申报产品名称。
使用境外实验室出具的检验报告,应当同时提交由相关实验室出具的送检样品与检验报告相对应关系的证明文件。
境外实验室出具的检验报告中已明确送检样品与检验报告相对应关系的(如境外实验室出具的检验报告中已注明产品名称,且产品名称与送检样品名称一致),不须另行出具送检样品与检验报告相对应关系的证明文件。
(3)申请变更化妆品行政许可检验报告中的生产企业名称、生产企业地址、产品中文名称的,相关许可检验机构应分别出具相应的补充检验报告并说明理由。
7、产品在生产国(地区)或原产国(地区)生产和销售的证明文件,应当符合以下要求:
(1)由产品生产国(地区)或原产国(地区)政府主管部门或行业协会出具。无法提交文件原件的,可提交复印件,复印件应经出具机构或我国使(领)馆确认。
(2)应载明产品名称、生产企业名称、出具文件的机构名称并有机构印章或法定代表人(或其授权人)签名及文件出具日期。
(3)所载明的产品名称和生产企业名称应与所申报的内容完全一致;如为委托加工或其他方式生产,其证明文件所载明的生产企业与所申报的内容不一致时,应由申请人出具证明文件予以说明;必须配合使用的多剂型产品可仅提交产品进口部分的生产和销售证明文件。
(4)生产和销售证明文件如为外文,应译为规范的中文,中文译文应由中国公证机关公证。
8、申报产品属于下列情况的,除按以上规定提交资料外,还应当分别提交下列资料:
(1)申报产品以委托加工方式生产的,应当提交以下资料:
1) 委托方与被委托方签订的委托加工协议书。
2) 进口产品应提交被委托生产企业的质量管理体系或良好生产规范的证明文件或符合生产企业所在国(地区)法规要求的化妆品生产资质证明文件。
3) 境内生产企业委托境外企业生产的进口产品可不提交行政许可在华申报责任单位授权书、生产和销售的证明文件及产品原包装,应提交产品包装设计。
4) 被委托生产企业的质量管理体系或良好生产规范的证明文件或符合生产企业所在国(地区)法规要求的化妆品生产资质证明文件应当符合下列要求:
① 由认证机构或第三方出具或认可。无法提交原件的,可提交复印件,复印件应由中国公证机关公证或由我国使(领)馆确认。
② 所载明的生产企业名称和地址应与所申报的内容完全一致。
(2)实际生产企业与化妆品生产企业(申请人)属于同一集团公司的,应提交实际生产企业与化妆品生产企业(申请人)属于同一集团公司的证明文件和企业集团公司出具的产品质量保证文件。
9、多个实际生产企业生产同一产品可以同时申报,其中一个实际生产企业生产的产品应按上述规定提交全部资料,此外,还应当提交以下资料:
(1)涉及委托生产加工关系的,提交委托生产加工协议书,进口产品还应提交被委托生产企业质量管理体系或良好生产规范的证明文件或符合生产企业所在国(地区)法规要求的化妆品生产资质证明文件。
(2)生产企业属于同一集团公司的,提交生产企业属于同一集团公司的证明文件及企业集团出具的产品质量保证文件。
(3)其他实际生产企业生产产品原包装。
(4)其他实际生产企业产品的卫生学(微生物、卫生化学)检验报告。
(5)其他实际生产企业化妆品使用原料及原料来源符合疯牛病疫区高风险物质禁限用要求的承诺书。
10、符合以下包装类型的样品应当按下列规定申报:
(1)一个样品包装内有两个以上(含两个)独立小包装或能分隔的样品(如眼影、粉饼、腮红等),且以一个产品名称申报,应分别提交产品配方和检验报告;非独立包装或不能分隔的样品,应提交一份检验报告,各部分应分别提交产品配方。
(2)样品为不可拆分的组合包装,且以一个产品名称申报,其物态、原料成分不同的,应分别提交产品配方、检验报告。
(3)两剂或两剂以上必须配合使用的产品,应按一个产品申报。根据多剂型是否混合后使用的实际情况,提交混合检验报告或分别提交各自剂型的检验报告。
(4)同一生产企业申报的2个或2个以上原包装外文名称相同,但外观形态不同的进口产品,应在申请表和生产销售证明文件外文名称中增加表示产品外观形态的词语,以示区别,并附相关说明。
11、多色号系列防晒化妆品,当基础配方相同,并申请抽样进行防晒功能(SPF、PFA或PA)检验时,可作为一组产品同时申报。每个产品申报资料中均应附上系列产品的名单、基础配方和着色剂一览表以及抽检产品名单。
12、境内企业委托境外企业生产加工的进口样品,按国产产品提交送审样品。
==========================================
以上可能有些复杂主要是想让进口化妆品的企业或个人都明白,如果不是很清楚可以看以下的八步动作,
第一步:明确产品情况和进口程序,预算周期及费用
(1)明确产品情况
作为化妆品产品的进口商,尤其是中国境内的经销商,一旦确定进口某个品牌的化妆品,应该首先明确该产品的实际情况,也是产品能够获得批准的前提条件,如:
该产品在生产国是否已经上市销售?该产品配方原料等是否符合中国大陆法规?该产品是否已在中国境内批准上市?产品属于非特殊还是特殊产品类别?
(2)了解进口程序、周期及费用
了解产品的同时,还应该知道,国外化妆品进口到中国大陆销售,主要需要经过两步:第一步就是向中国国家食品药品监督管理总局(CFDA)申请行政许可批件/备案凭证,这是进口的先决条件;获取该批件/凭证后,第二步即可进行正常的报关报检了。
下面说说第一步所需的时间及费用预算情况。
申请周期是广大客户最关心的问题之一, 根据天健华成公司的经验,进口非特殊类化妆品一般可在3至6个月内完成申报,获得备案凭证。进口特殊类化妆品,根据不同功能,整个申报周期约为6~12个月左右。
第二步:签订代理合同,确定外方资料提供情况
经过前面的考察了解之后,就进入实质操作阶段了。
作为经销商,应该和国外生产企业签订产品代理合同,CFDA批文有效期是4年,所以代理合同的期限最好在4年以上。
签订合同的同时,应了解外方是否能够提供产品相关技术文献(如完整配方、工艺、质量标准等)和证明文件(如销售证明等),因为不排除有些国外企业出于知识产权保护不愿提供个别技术核心资料。
另外,对欧洲国家的产品还应确定外方是否同意动物实验,因为欧洲国家是不提倡动物实验的,而在CFDA审批过程中,动物实验是必做项目。
需要获取的产品资料及其要求,或CFDA官网相关信息。委托天健华成代办的话,可以简省提供资料并可获得相关样本帮助。
第三步:确定申请方式,自主申请还是委托代理
由于目前进口化妆品注册申请的专业性越来越强,难度越来越大,所以申请企业只能有两个选择:要么配备专业注册人员或部门,要么委托像天健华成公司这样的专业代理机构。对一些产品尚未正式运营的公司来说,配备专门的部门或人员显然不太现实,那么如何选择一家合适可靠的代理机构就成为关键问题。。
第四步:授权书备案,正式申请的开始
授权书备案是进口化妆品行政许可批文正式申请的第一步。备案完成之后,才能继续下面的样品检测、送审等程序。授权书是指国外化妆品生产企业向在华申报责任单位(可为经销商、外商分公司等)的授权,授权书应由申请人和在华申报责任单位共同签署,并经公证机关公证后向CFDA提交备案;授权书为外文的,还应译成中文,并对中文进行公证。
第五步:检测样品
授权书备案完成后,按相关要求准备好送检资料及样品,送交CFDA认可的检测机构进行检测,根据产品功能和配方的不同,一般20天至6个月左右出具检测报告。具体检测项目、周期及费用可参。
第六步:递交申请
完成样品检测后,根据《化妆品行政许可申报受理规定》(国食药监许[2009]856号)等法规整理送审文件成册后,向CFDA受理中心提出申请。受理机构接收化妆品行政许可申报资料后,在5个工作日内对申报资料进行形式审查,并作出是否受理或补正的决定。
第七步:资料补正
形式审查及技术审查(评审)后,如有提出补正意见,应按要求进行补正。
第八步:获取批文
进口化妆品从受理到获批的行政周期为20日(普通类)至110日(特殊类),但由于存在补正等环节,所以实际获取批文的周期通常高于上述行政周期。批文获取后,其有效期为4年,到期后可进行延续。
至此,您的产品就可以进行正常报关、销售等手续了。