受全球疫情爆发影响,口罩及其他疫情物资抢购再一次推上疫情浪尖。近期,陆续接到客户关于口罩出口报关方面的业务咨询,也会涉及是否会被海关扣押等敏感话题。中国并未禁止口罩出口报关,也没有任何海关方面禁止口罩出口的新闻和书面通知禁止,口罩出口报关时被限制、被误会,根本原因在于出口资质和海外的要求不同。
以下针对口罩等疫情物资的进出口问题,收集和整理了一些要求和规范,希望能帮助到疫情物资进出口企业。
欣创口罩出口报关咨询:
联系人:李凯天
手机/微信:13580891024
邮件:chrisle@xichung.com
QQ:297309909
1
口罩医用与非医用的区别
民用口罩送进了医院,对于医护人员会是多么危险的事情。 3月31日,商务部会同海关总署、药监局发布《关于有序开展医疗物资出口的公告》(2020年第5号),要求出口医用口罩等5类产品必须取得国家药品监管部门相关资质,符合进口国(地区)质量标准要求。 各国标准不同,我们怎么避免医用民用颠倒,如何避免类目错误清关失败呢?
1
从用途看,分为医用和非医用
1)医用分为:医用防护、医用外科、一次性医用 (普通医用口罩的英文是 medical masks) (医用外科口罩的英文是 surgical masks) (一次性医用口罩的英文是:Disposable Medical/surgical masks) 2)非医用分为:防颗粒物、日常防护
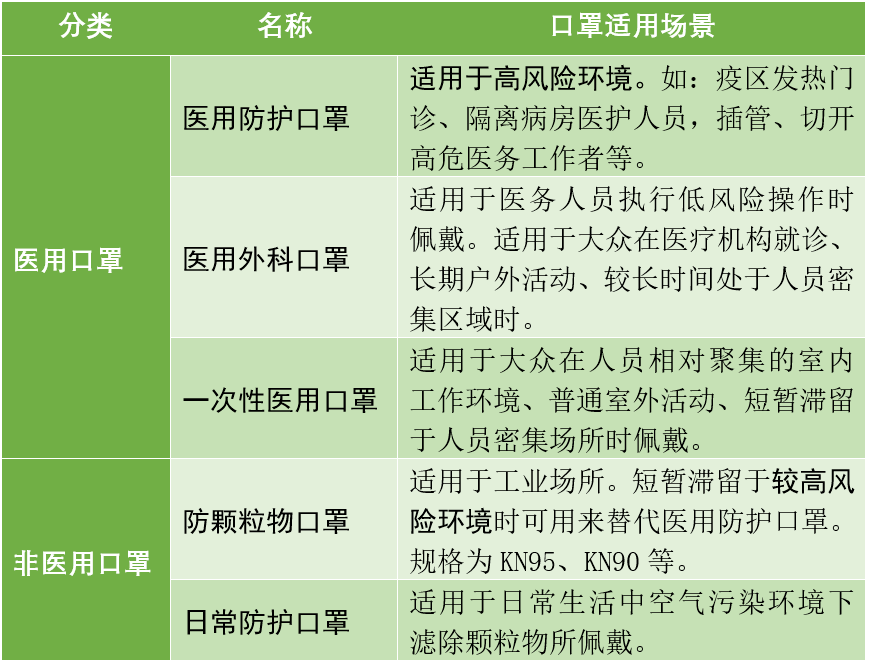
可以根据我国及国外口罩相关标准进行区分:

参考文件:
http://www.xinhuanet.com/tech/2020-02/02/c_1125521311.htm
3层平面罩类似平时我们带的蓝色那种,KN95是中国标准GB2626-2006中规定的级别,而N95是美国标准42-CFR-84中规定的级别。
2
从结构来看
3
从包装来看
正规途径的口罩产品的最小单元包装上应该有商品名称、执行的标准和防护等级等信息。这些商家明示的信息可以作为一个分辨点,如商品名称中带有“医用”或英文“surgical”“Medical”等字样的,一般可判定为医用口罩。
4
各国从使用标准区分
医用口罩在美国适用《医用口罩材料性能标准规范》(ASTM F2100),由美国食品药品监督管理局(FDA)管理,须通过501K注册或近期FDA公布的其它途径,获得工厂注册和医疗器械列名后方可在美国上市。因此美国客户经常问的FDA 属于医用口罩。
FDA 证书查询:
https://www.accessdata.fda.gov/scripts/cdrh/cfdocs/cfPMN/pmn.cfm
另外根据FDA最新政策,目前是在满足一定条件的情况下认可中国标准的口罩,其授权企业的链接为:
https://www.fda.gov/media/136663/download
美国非医用口罩不属2020年第5号公告范围,但企业应注意,产品需通过NIOSH注册方可在美国销售。
2)欧盟
欧盟医用/非医用口罩均需有CE认证,但适用标准不同。
医用口罩在欧盟属于I类器械,分为I类非无菌和无菌两种,需按照欧盟医疗器械指令93/42/EEC(MDD)或欧盟医疗器械条例EU2017/745(MDR)加贴CE标志。
需要注意的是,根据口罩无菌/非无菌状态,欧盟采取不同的合格评定办法,非无菌医用口罩企业只需进行CE自我符合性声明,不需要通过公告机构认证。在准备好相应文件及测试报告等资料后,即可自行完成符合性声明。无菌医用口罩还必须由授权公告机构进行CE认证。
出口欧盟医用口罩可通过获得授权的公告机构进行查询,其中欧盟医疗器械指令93/42/EEC(MDD)授权的公告机构查询地址为:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=13
欧盟医疗器械条例EU 2017/745(MDR)授权的公告机构查询地址为:
https://ec.europa.eu/growth/tools-databases/nando/index.cfm?fuseaction=directive.notifiedbody&dir_id=34
其他国家和地区,一般情况下FDA CE 认证也认可。订单洽谈与进出口报关看具体情况。
除常规的箱单发票外,国内出口贸易企业需具备的资质和材料:
1. 营业执照(经营范围有相关经营内容)。 2. 企业生产许可证(生产企业)。
3. 产品检验报告(生产企业)。
4. 医疗器械注册证(非医用不需要)。
5. 产品说明书(跟着产品提供)、标签(随附产品提供)。
6. 产品批次/号(外包装)。
7. 产品质量安全书或合格证(跟着产品提供)。
8. 产品样品图片及外包装图片。
9. 贸易公司须取得海关收发货人注册备案。
1
国内出口口罩生产企业资质证明
生产属于医疗器械管理的口罩用于出口,中国海关不需要企业提供相关资质证明文件,但一般进口国会要求生产企业提供产品三证,以证明该进口的商品在中国已合法上市,具体如下:
1. 营业执照(经营范围包含有医疗器械相关,非医疗级别的物品不需要)。 2. 医疗器械产品备案证或者注册证。
3. 厂家检测报告(合格证)。
生产企业有进出口权,可以自行出口,如没有进出口权,可以通过外贸代理进行出口销售。
2
内贸企业做出口需要取得的基本资质
1. 向市场监管部门取得营业执照,增加经营范围“货物进出口、技术进出口、代理进出口”。
2. 向商务部门取得进出口权,可直接在商务部业务系统统一平台
(http://iecms.mofcom.gov.cn/)申请,网上提交材料。
3. 向外汇管理局申请取得开设外汇账户许可。
4. 办理进出口货物收发货人海关注册登记。
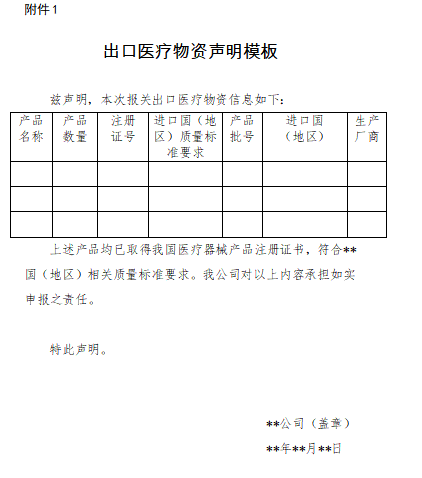
根据《医疗器械分类目录》(国家食品药品监督管理总局公告 2017年第104号),医用口罩属二类医疗器械。报关时需按照《商务部 海关总署 国家药品监督管理局关于有序开展医疗物资出口的公告》(2020年第5号)要求,提供医疗器械产品注册证和出口医疗物资声明。
1
报关前提条件
收发货人注册编码(慈善机构可为临时编码),需办理无纸化通关法人卡(一般在海关处办理)。
出口口罩时,应关注国外哪些准入要求?
不同国家对进口口罩要求不同,如美国对进口医用口罩需要FDA注册,欧盟对进口非医用口罩要求获得CE认证等
2
出口申报要求
1)商品归类:除特殊情况外,绝大部分口罩应归入的税号可查询www.hsbianma.com
2)检验检疫:若口罩为非法检产品,申报时检验检疫项目无需填报。根据我国政府与相关国家签订的政府间检验协议,对出口伊朗等少数几个国家的产品需按规定进行装运前检验。
3)关税征免:如出口物资为贸易性质,征免性质申报一般征税,征免方式申报照章征税;如为捐赠性质,境内发货人为贸易代理商、慈善机构等,征免性质可不填,征免方式申报全免。
4)申报规范:按照规范申报要求填写商品名称、成份含量,严格遵守单单一致单货一致原则;如物资非中国生产,原产国按照实际生产国填写。
5)口罩的出口退税率为13%。
3
报关到底需要些什么资料
大多数人,都是摸着石头过河,在疫情之前压根没碰过口罩,加上海关政策天天在变。所以,我们在口罩出口的时候,最好跟对应的货代确认清楚,下面以几家货代提供的信息为例供大家参考。
1)
2)目前,截止4月14日,货代要求我们提供的资料为:
非医用出口要求:
1. 营业执照,工商营业执照需具备“特种劳动防护用品制造”(具体以市场监督管理局核定为准)的经营范围。 2. 产品说明书、标签。
3. 产品批次/号
4. 产品质量安全书
5. 产品样品图片及外包装图片
6. 产品合格证
7. 内贸合同- 经营单位跟生产厂家购买的依据
3)单证一般贸易报关提供以下:
1. 提供:箱单、发票、合同、报关草单、货物图片(含包装图片、和口罩图片)、电子委托。 2. 品名需按机场海关规范申报:XX牌XX型号医用/非医用口罩
3. 不同牌子,不同型号要分开不同项申报,不能混合
4. 净重要按实际称重申报,单价要按实际市场成交价申报。
5. 申报计量单位须为:“个”
6. 医用的话请提供营业执照、医疗器械注册备案证、医疗器械生产许可证
7. 出口医疗物资声明(格式如附件)(一般货代会提供)
按照《中华人民共和国进出口商品检验法》及其实施条例,海关总署决定自本公告发布之日起,对“6307900010”等海关商品编号项下的医疗物资(详见附件)实施出口商品检验。
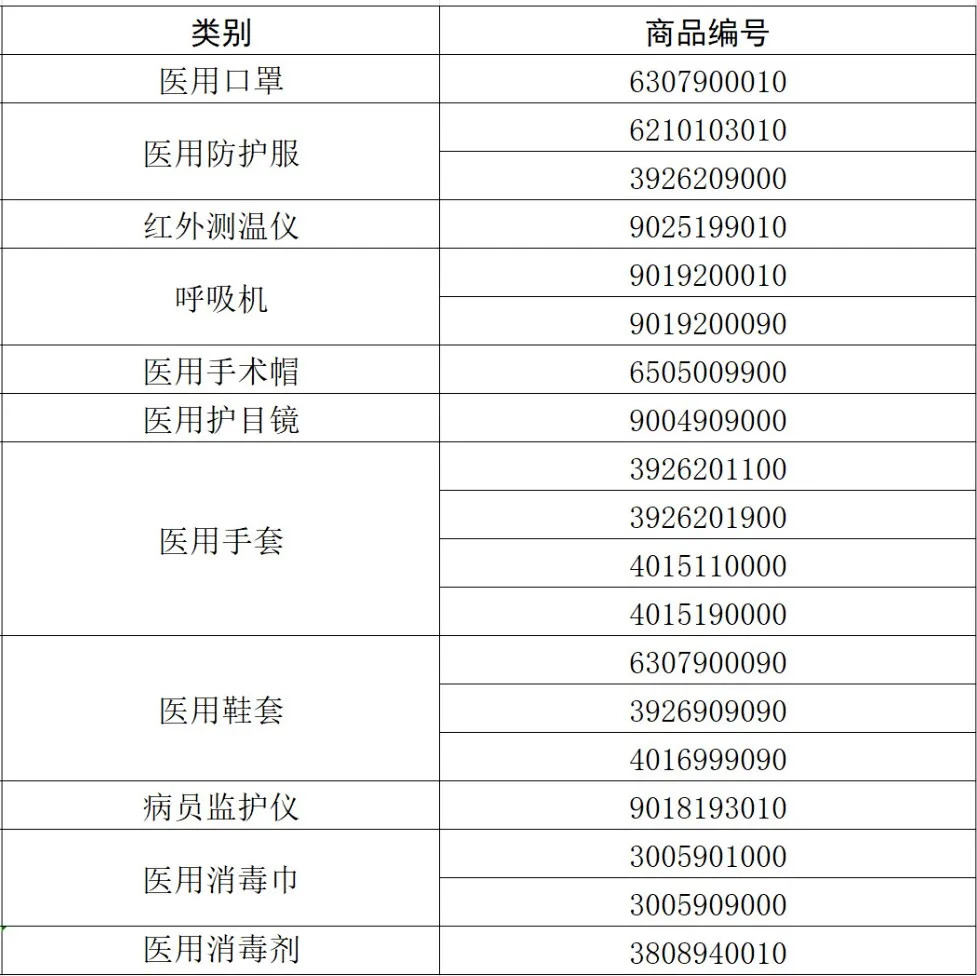
1. 只有上述HS编码项下医用商品才实施出口法检,非医用不实施出口法定检验。
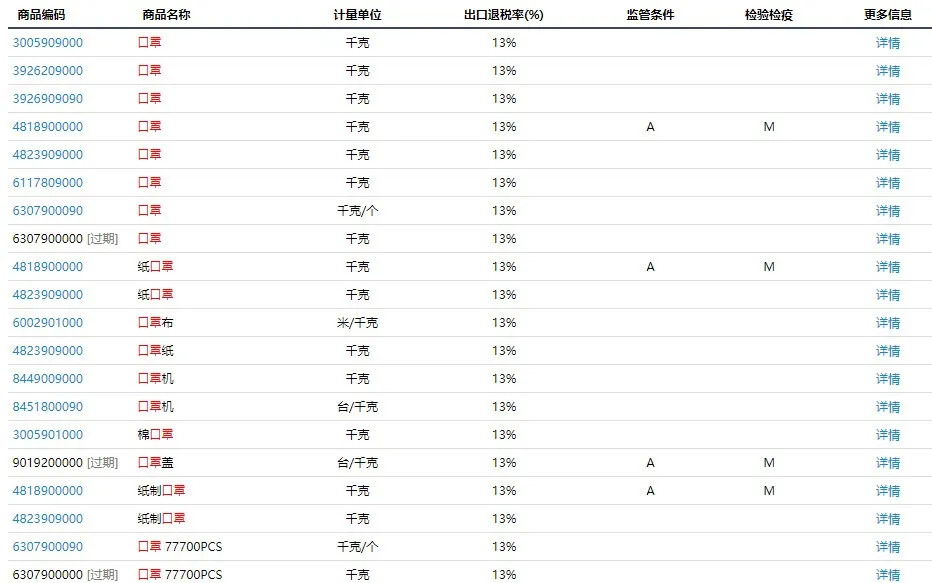
2. 医用口罩出口属法检商品,报关前是否需要申请电子底账?
与其它出口法检商品不同,此次新增纳入《法检目录》的11类医疗物资,在出口前不需要申请电子底账,正常向海关报关,报关时不需提供电子底账号。当然,也不实施产地检验,无需在产地报检。
3. 医用口罩出口时,在口岸检验的内容有哪些?
《医疗器械监督管理条例》第四十四条规定“出口医疗器械的企业应当保证其出口的医疗器械符合进口国(地区)的要求”。
《商品检验法》第六条规定“必须实施的进出口商品检验,是指确定列入目录的进出口商品是否符合国家技术规范的强制性要求的合格评定活动。合格评定程序包括:抽样、检验和检查;评估、验证和合格保证;注册、认可和批准以及各项的组合。
医用口罩出口时,海关根据风控指令要求实施现场合格评定:
a. 验证实货是否与医疗器械注册证一致; b. 检查商品包装、标识、品名、数量以及是否冒用、伪瞒报等;
c. 对企业提交的质量安全承诺书(合格保证)或检测报告进行评定;
d. 检验商品外观质量检验;
e. 抽样送实验室对商品的内在质量进行检测;
4. 如何看待商检
很多人一听说法检,瞬间慌了,实际上来讲商检并没有我们想象中的那么困难。
所谓真金不怕火炼,只要物品合格,都是可以正常出口的。跟报关类似,配合货代,填写报检委托书等相关信息就行,从流程上来讲并不是很复杂。
那商检之具体有哪些不利于企业/外贸人员的呢?
一个是商检需要一定时间,增加了货物出口的速度,以及允诺给买家的交期。
第二个,三无产品就不用说了,商检肯定过不了,那么整批货都有风险。所以奉劝各位不要被一时诱惑冲昏头脑得不尝失,医用类别一定要按质按量要标准出口。
(以下两张图表,供生产企业参考)
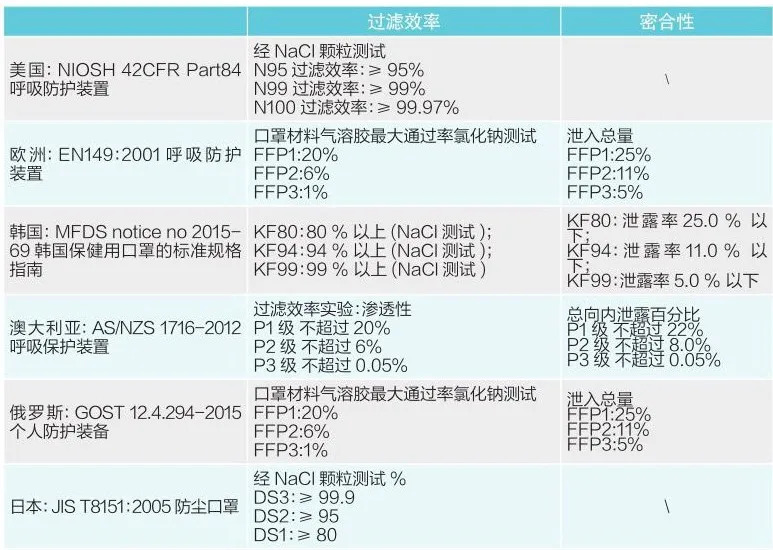
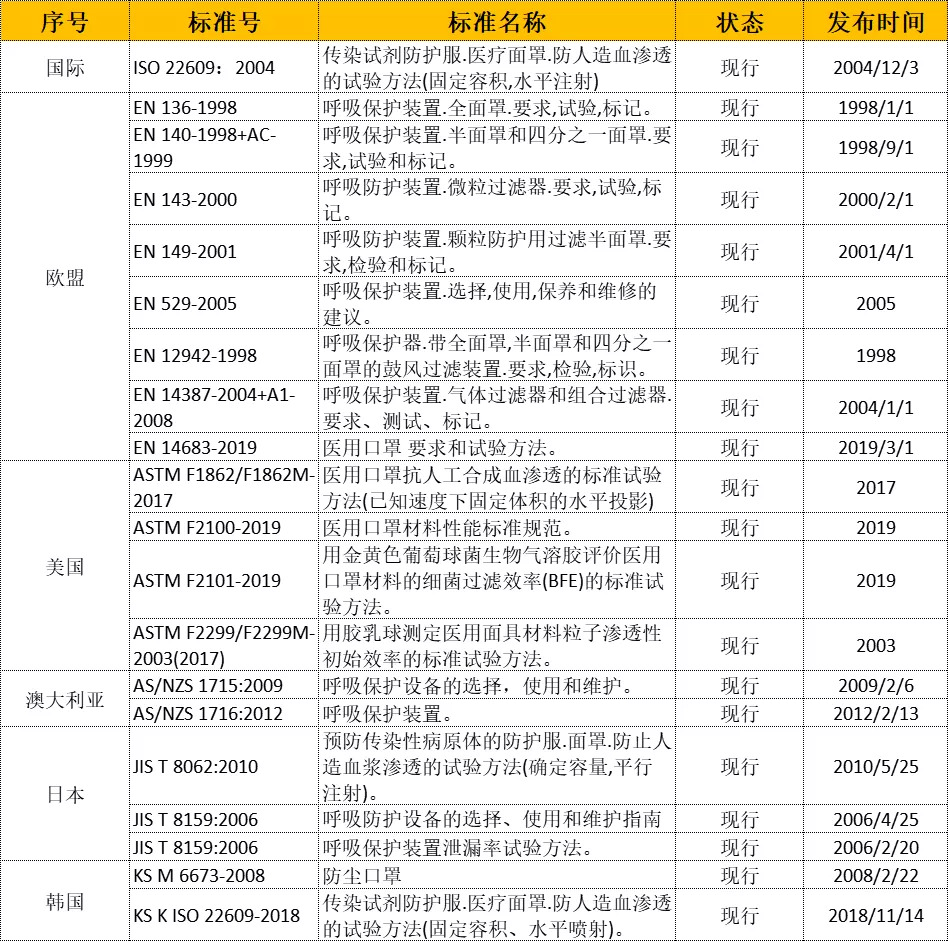
订单洽谈前后,最好也跟货代确认,货物出口过程中对包装有哪些要求。
1、可直接销售的最小包装(塑料包装袋或纸盒包装)上印刷标签和产品图片;
(1)必有信息:
①产品名称、②规格型号、③生产地、④经营单位或生产企业名称、⑤执行标准号(例GB19083-2010)、⑥有效期、⑦数量;
(2)其他可有信息:
①滤料级别或相应说明、②使用前请参见使用说明或其他说明、③用途(功能、适用范围)、④贮存条件、⑤一次性使用产品应标明“一次性使用”或相当字样、⑥如为灭菌产品应注明灭菌有效期及灭菌方式等。

2、外包装(出口纸箱)上内容为:
①MADE IN CHINA、②品名、③经营单位或生产企业名称、④“非医用”
很多小伙伴遇到买家自行提供DHL 账户要样品的情况。这时候一般国外客户会给我们他的账号,外贸人们屡屡在这上面遇到问题,那下次一客户到付账户DHL 官方寄样品的就往下看吧:
第一步:点击打开DHL eship 登录或注册账户:Eship.cndhl.com

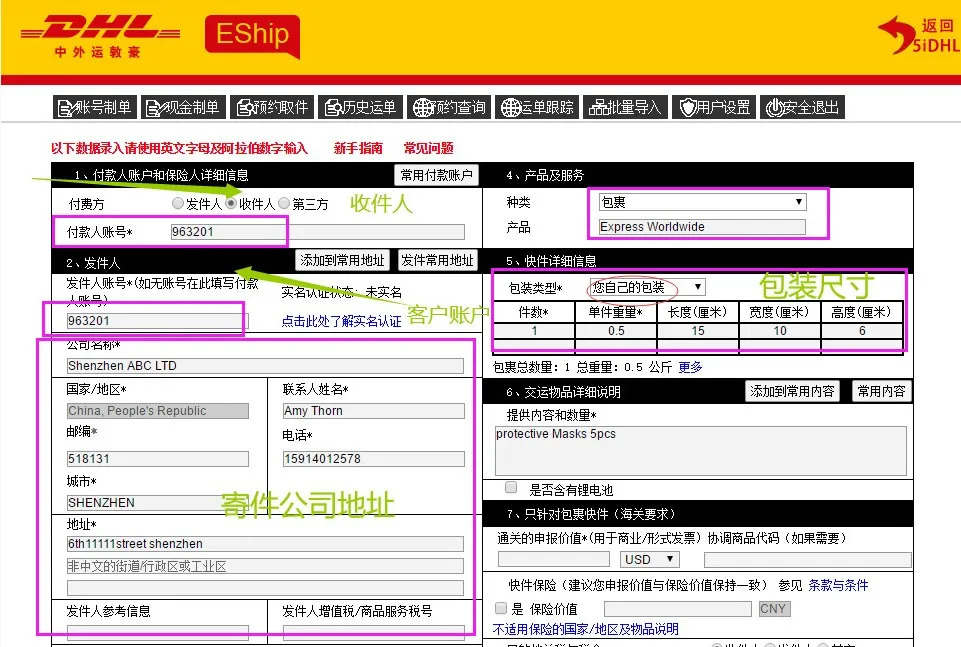
第二步:填写相关信息
1. 付款账号,按照实际谁付款来选择 2. 填写发件人信息和收件人信息
3. 包装类型选择和包装尺寸填写
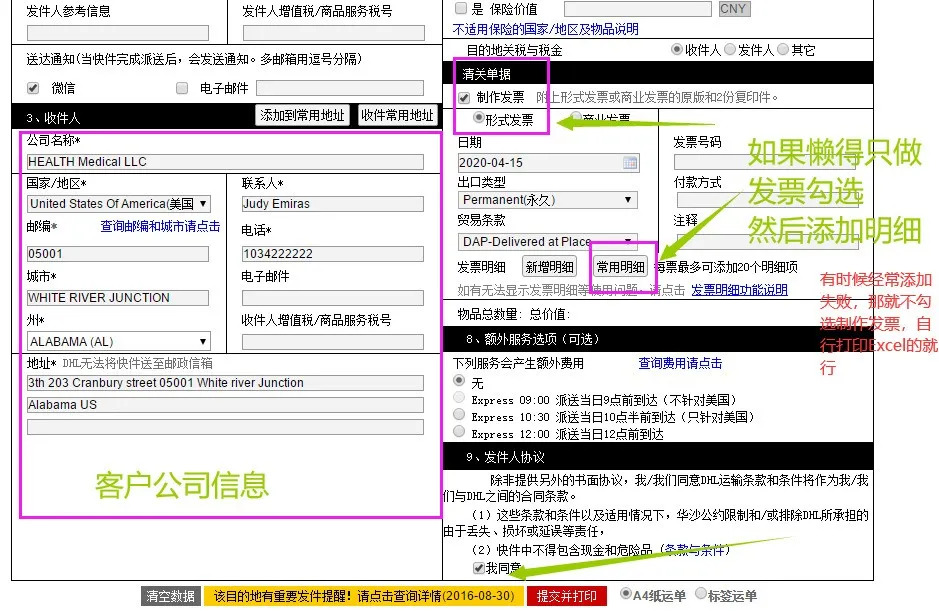
4. 是否要制作发票
这里为了避免发票添加明细失败,可以直接用自己的CI 打印2份。所以直接不制作发票即可。
如果不想重新制作发票,勾选以后新增明细也可以,但是我们自己操作的时候经常添加明细失败。
5. 同意,提交就可以
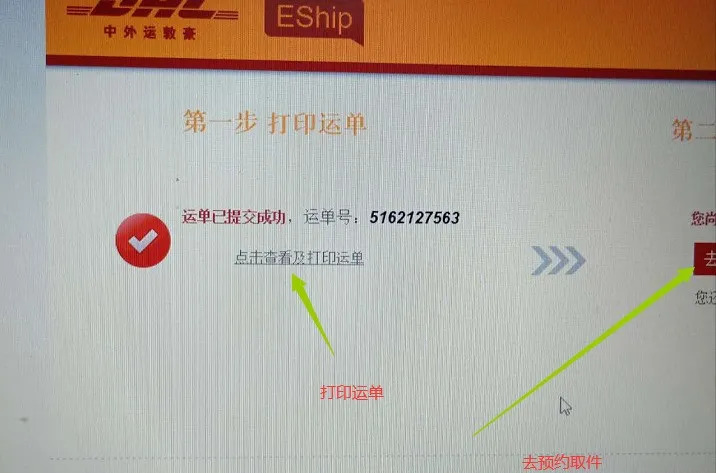
第三步,打印运单!!!(很多人忘记)然后点右边第二步,预约取件